近日,中国农业科学院上海兽医研究所家禽病毒病监测预警和防控团队揭示了新城疫病毒(NDV)通过诱导细胞内游离钙离子(Ca²⁺)升高导致线粒体氧化应激和功能损伤,造成线粒体膜通透转换孔(mPTP)开放,介导线粒体凋亡诱导因子(AIF)的释放并入核,触发细胞发生非Caspase依赖的帕特农死亡(Parthanatos),相关研究结果发表在《PLOS Pathogens》上。
细胞凋亡是一个程序性细胞死亡的过程,受到一系列复杂途径的严格调控,被认为是一种自杀行为,旨在消除不需要的和潜在危险的细胞。细胞凋亡既可以通过细胞死亡受体介导的外源性途径启动,也可以通过与线粒体功能障碍相关的内在途径启动。这些进程均需要依赖半胱氨天冬氨酸蛋白水解酶家族(Caspase)。Parthanatos是一种不依赖Caspase蛋白家族,而是通过诱导AIF的核转位直接造成细胞核DNA大量片段化(20-50 kb)而导致细胞死亡的方式,其主要表现形式是PARP1过度激活和PAR聚合物积累。
该研究发现NDV感染导致线粒体病理性Ca²⁺大量积聚,且这些钙离子主要来自于细胞钙库—内质网的钙波急性释放。线粒体过量积累的钙离子导致线粒体氧化应激、结构损伤和功能丧失,促进了AIF从线粒体释放,造成DNA断裂和细胞死亡。研究还发现,ROS作为氧化应激的产物,和钙信号一样在细胞凋亡进程中也起到了关键作用。细胞内Ca²⁺的增加有助于NDV感染诱导的ROS的积累,清除ROS也能够显著降低NDV诱导的细胞质和线粒体Ca²⁺的升高。这项研究发现了Ca²⁺和ROS通过Ca²⁺-线粒体-ROS信号轴介导NDV诱导的AIF依赖性的Parthanatos死亡的调控机制。该研究深化了对Ca²⁺在病毒感染进程中信使作用的认知,从功能离子组学角度对病毒诱导细胞死亡发生机制解析提供了新的见解,有助于更深入地了解NDV分解肿瘤的新机制,并为未来的抗病毒研究提供了有价值的见解。
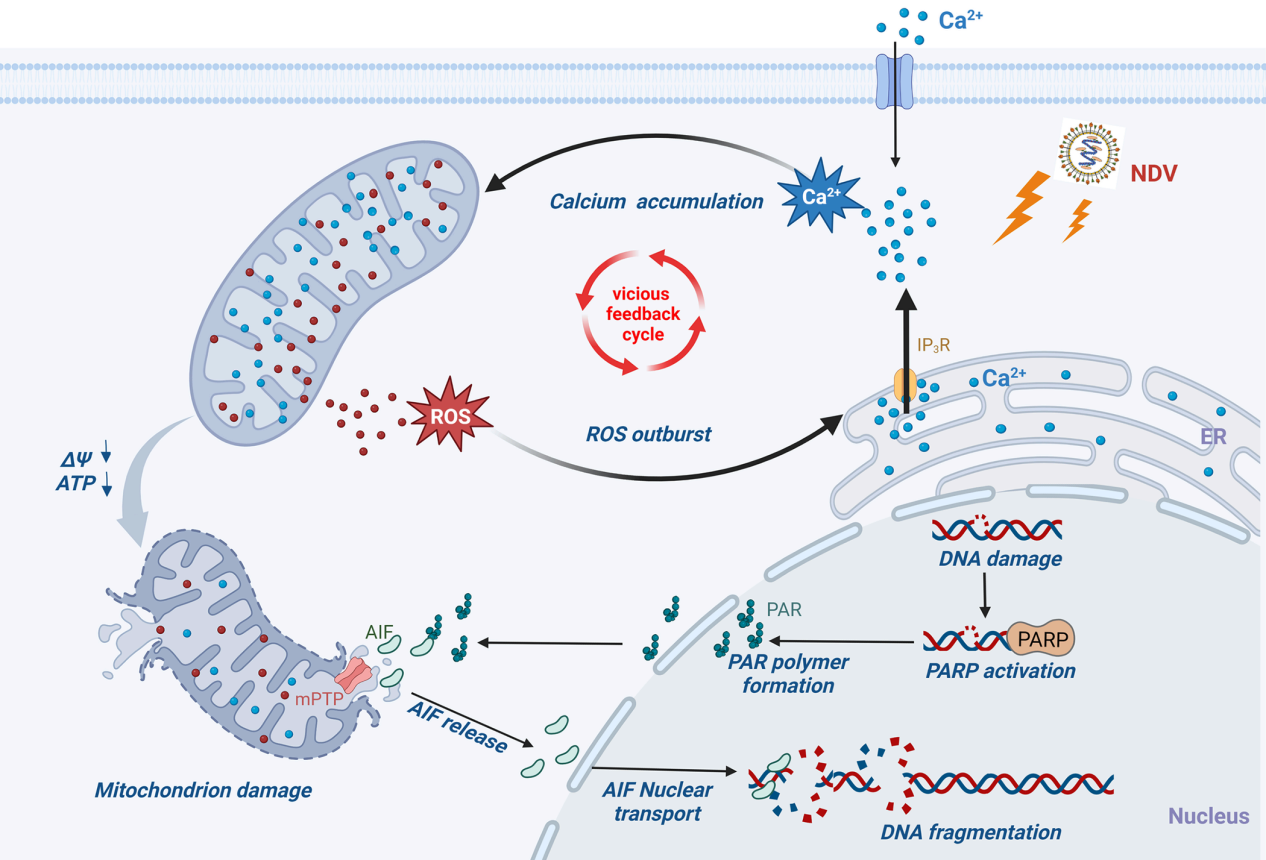
NDV通过钙-线粒体-活性氧信号轴诱导Parthanatos的模式图
中国农业科学院上海兽医研究所博士后屈阳为论文第一作者,上海兽医研究所丁铲研究员、孙英杰研究员和西北农林科技大学杨增岐教授为论文共同通讯作者。该研究得到国家自然科学基金重点项目和国家重点研发计划项目支持。
原文链接:https://journals.plos.org/plospathogens/article?id=10.1371/journal.ppat.1012737




