近期,中国农业科学院上海兽医研究所动物源性食品安全研究团队发现壳聚糖通过调节TLR4/STAT1信号通路和肠道菌群,提升免疫抑制小鼠对微小隐孢子虫感染的抵抗能力,显示了壳聚糖在预防和治疗寄生虫感染方面的潜在应用价值,也为探寻微小隐孢子虫感染新的治疗靶点提供了思路。相关研究在线发表在免疫学期刊Frontier in Immunology上。
隐孢子虫是一种世界性分布的重要食源性寄生虫,是导致儿童腹泻的第二大病原体,可引起持续腹泻,甚至危及生命,并与儿童发育迟缓和认知障碍有关。美国食品和药物管理局(FDA)批准用于隐孢子虫病治疗的唯一药物是硝唑尼特,但该药对婴儿和免疫缺陷病人等易感宿主无效。因此,探寻安全有效的抗隐孢子虫病药物迫在眉睫。
近年来,不少学者将关注点聚焦于天然药物的抗隐孢子虫作用。壳聚糖是一种无毒性多糖,主要来源于甲壳类动物和虾。壳聚糖纳米颗粒常被用作药物的传递载体,对包括隐孢子虫病在内的原虫病,以及真菌病、细菌病等疾病显示出良好的治疗效果,但其作用机制尚不清晰。
本研究通过口服壳聚糖制剂,观察其对免疫抑制小鼠血液生化指标、细胞因子、重要信号通路分子及肠道微生物种群的调节作用。结果发现,壳聚糖可增加隐孢子虫感染小鼠的体重,减轻病原感染造成的运动迟缓、毛发皱褶、运动减少、食欲减退等症状;改善感染小鼠血液中白蛋白、血清碱性磷酸酶(ALP)、谷丙转氨酶(ALT)和 谷草转氨酶(AST)等生理生化指标;极显著降低感染小鼠体内排出的隐孢子虫卵囊。此外,补充壳聚糖可极显著降低感染小鼠的干扰素(IFN-γ)和肿瘤坏死因子(TNF-α)mRNA的转录水平( p<0.01),降低细胞因子风暴对宿主造成的损害;极显著抑制TLR4蛋白的表达水平,而上调STAT1蛋白的表达水平( p < 0.01) 。同时,壳聚糖可缓解感染小鼠肠道内细菌多样性的减少,增加了拟杆菌门/拟杆菌属细菌的相对丰度,而变形菌、软壁菌、脱铁杆菌和厚壁菌的相对丰富度显著降低。由于壳寡糖作为氨基多糖的降解产物,是肠道微生物的重要营养来源,推测其对肠道微生物种群起到保护和维持作用。上述研究结果表明,壳聚糖可通过重塑小鼠肠道菌群的组成,上调STAT1信号通路,下调TLR4信号通路及IFN-及和TNF-α的表达,从而减轻微小隐孢子虫感染造成的损害。
该研究得到上海市科技兴农项目、上海市科委科技创新行动计划实验动物研究领域项目等的资助。中国农业科学院上海兽医研究所动物源性食品安全研究团队巴基斯坦籍博士生Sajid Ur Rahman为本文第一作者,陈兆国研究员为通讯作者,中国农业科学院上海兽医研究所为唯一完成单位,课题组成员龚海燕、米荣升、黄燕和韩先干等人参与了研究工作。
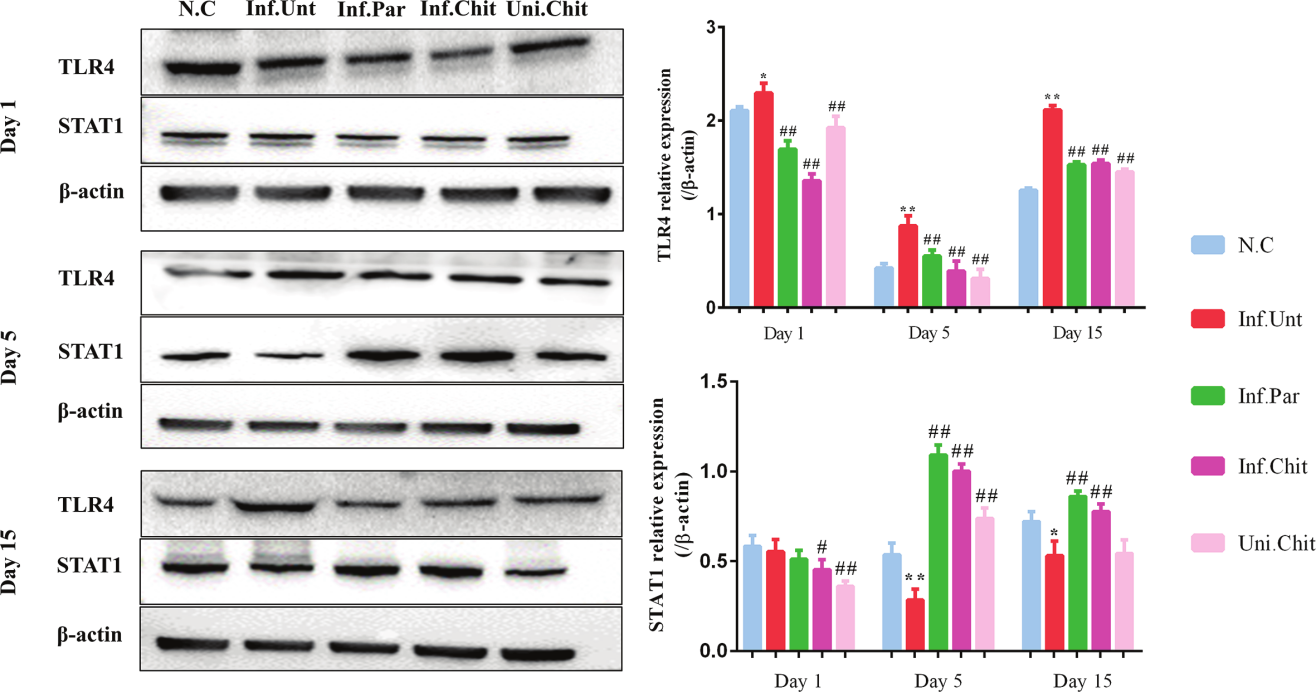
壳聚糖显著抑制TLR4却促进了STAT1蛋白的表达
原文链接:https://pubmed.ncbi.nlm.nih.gov/35095858/




